Fluor
Cześć, młody odkrywco! To fascynujące, że wybrałeś do zbadania jeden z najbardziej reaktywnych pierwiastków w całym układzie okresowym – fluor. Czy wiesz, że fluor, zajmujący dziewiąte miejsce w układzie okresowym, zawiera dziewięć protonów w swoim jądrze atomowym?
Sprawdź, gdzie znajdziesz ten pierwiastek w Układzie Okresowym Pierwiastków:
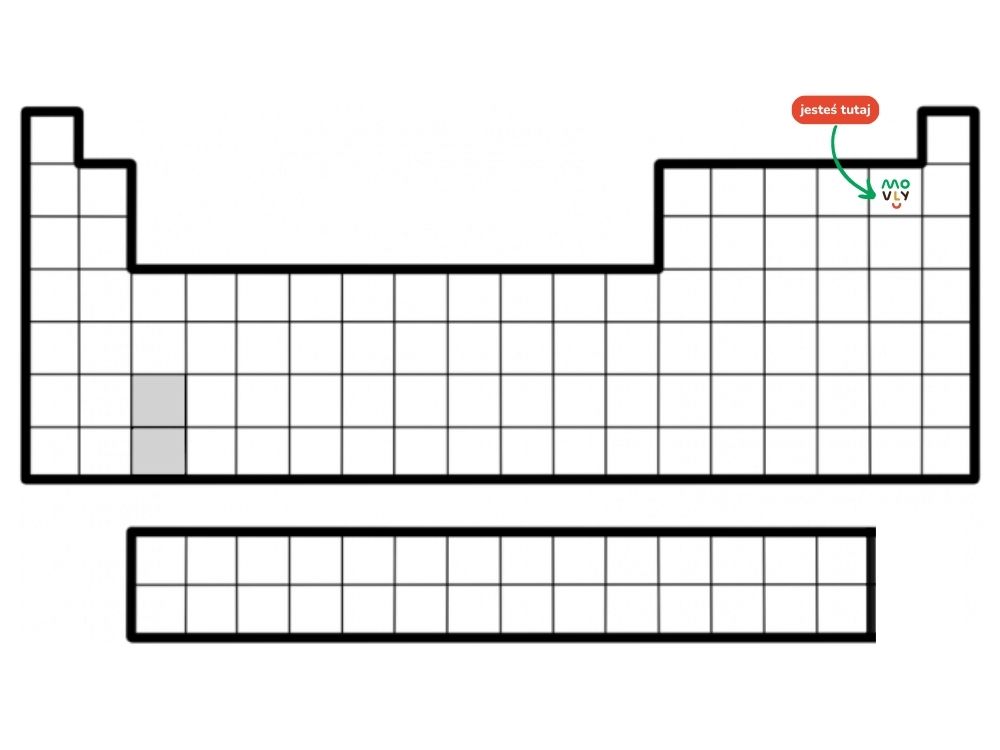
Historia odkrycia fluoru
Historia odkrycia fluoru jest zarówno ekscytująca, jak i pełna wyzwań. Pomimo wielu starań, fluor został odkryty dopiero w 1886 roku przez francuskiego chemika, Henri Moissana, głównie ze względu na swoją ekstremalną reaktywność, która utrudniała izolację czystego elementu.
Jak jest zbudowany atom fluoru?
Atom fluoru składa się z dziewięciu protonów, które nadają mu miejsce w układzie okresowym. Ma również dziesięć neutronów, które razem z protonami tworzą jądro atomu i dziewięć elektronów, które krążą wokół jądra. Ciekawe, prawda?
Zastosowanie fluoru w codziennym życiu
Fluor jest pierwiastkiem o szerokim zakresie zastosowań, od medycyny po przemysł. Oto kilka przykładów:
Stomatologia: Fluor jest kluczowym składnikiem past do zębów i płynów do płukania jamy ustnej, ponieważ pomaga zapobiegać próchnicy.
Przemysł chemiczny: Ze względu na swoją ekstremalną reaktywność, fluor jest wykorzystywany w wielu procesach przemysłowych, w tym produkcji wielu typów plastików.
Farmacja: Wiele leków zawiera fluor, który pomaga zwiększyć ich skuteczność.
Przemysł jądrowy: Fluor jest również ważny w przemyśle jądrowym, gdzie jest używany do produkcji paliwa jądrowego.
Serdecznie zapraszam Cię do dalszego odkrywania fascynującego świata fluoru!







